Induzierte Apoptose durch kalt atmosphärisches Plasma in menschlichen Dickdarm- und Lungenkrebszellen
durch Modulation des mitochondrialen Signalwegs
Autoren: Yanhong Wang, Xinyu Mang, Xuran Li, Zhengyu Cai and Fei Tan
Publikation: Cold atmospheric plasma induces apoptosis in human colon and lung cancer cells through modulating mitochondrial pathway, Frontiers in Cell and Developmental Biology, Front. Cell Dev. Biol., 26 July 2022, Sec. Cell Death and Survival
Zuerst veröffentlicht: https://www.frontiersin.org/articles/10.3389/fcell.2022.915785/full
Zusammenfassung:
Zusammenfassung einer interessanten Publikation zur Grundlagenforschung mit unserem Industrieprodukt piezobrush® PZ2 zum möglichen Einsatz im Medizinbereich:
Die Behandlung mit kaltem atmosphärischen Plasma (CAP) ist eine aufstrebende und vielversprechende Onkotherapie mit beträchtlichem Potenzial und Vorteilen, die traditionellen Behandlungsmodalitäten fehlen. Das Ziel dieser Studie war es, die Wirkung und den Mechanismus der Plasma-inhibierten Proliferation und der Plasma-induzierten Apoptose auf menschliche HT29-Darmkrebszellen und A549-Lungenkrebszellen in vitro und in vivo zu untersuchen.
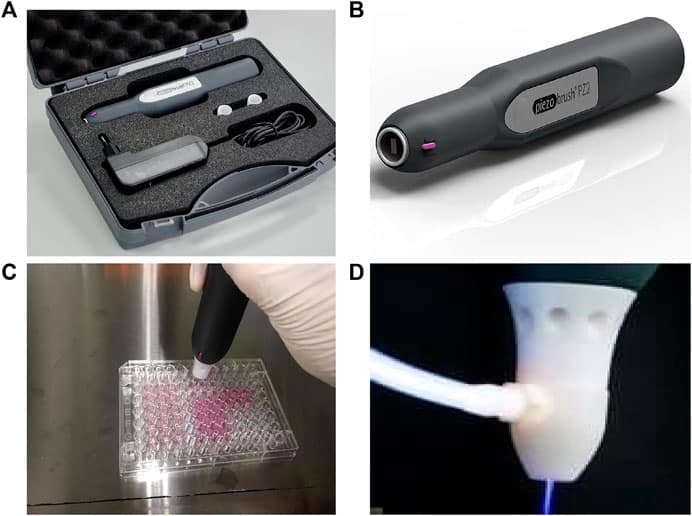
In dieser Studie wurde der piezobrush® PZ2 von relyon plasma, ein tragbares CAP-Gerät, das auf der piezoelektrischen Direktentladungstechnologie basiert, zur Erzeugung und Abgabe von nicht-thermischem Plasma verwendet. Das CAP-Gerät erzeugte bei einer maximalen Leistungsaufnahme von 30 W kalt aktives Plasma mit einer Düsentemperatur von <50 °C. Die Plasmadüse wurde 10 mm über der zu behandelnden Oberfläche platziert. Die Behandlungsdauer betrug 15, 30, 60 und 120 Sekunden (Abbildungen 1C, D). Um die Wirkung der PZ2-Behandlung auf verschiedene Tumorzellen zu untersuchen, wurde eine direkte Plasmabehandlung an den HT29- und A549-Zellen ohne Bedeckung durch das Zellkulturmedium durchgeführt.
Die Plasma-Behandlung hemmte die Proliferation von HT29-Darmkrebszellen und A549-Lungenkrebszellen. Die Untersuchung der hemmenden Wirkung der CAP-Behandlung wurde mit dem Cell Counting Kit-8 vorgenommen. Die verursachten morphologischen Veränderungen auf zellulärer und subzellulärer Ebene wurden unter Verwendung der Transmissionselektronenmikroskopie untersucht und die Tumorzellmigration und -invasion wurden mittels des Transwell-Migration- und Matrigel-Invasion-Tests durchgeführt.
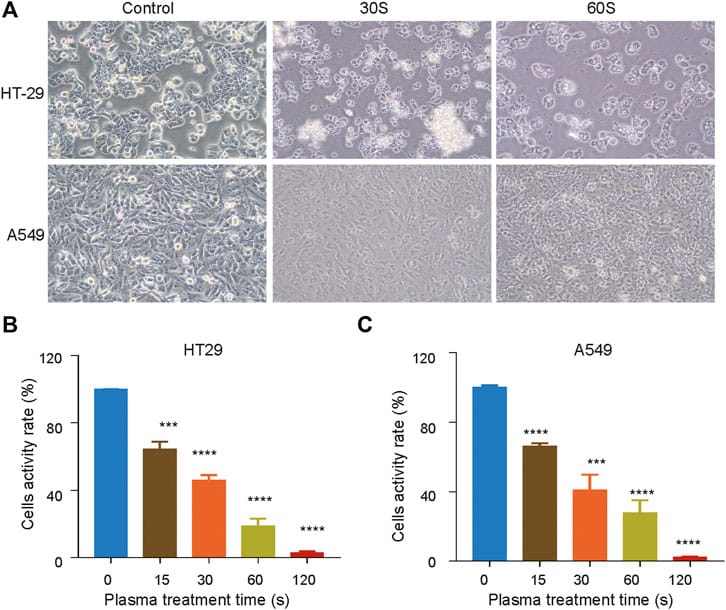
Die optischen Bilder (A) in Abbildung 2 zeigen die Schäden der HT29- und A549-Zellen, die durch die Behandlung mit dem piezobrush® PZ2 verursacht wurden. Die Bilder (B) und (C) zeigen die abnehmende Zellaktivität, während die Behandlungsdauer mit CAP zunimmt. Die obigen Bilder und Werte stellen Ergebnisse von drei unabhängigen Experimenten dar.
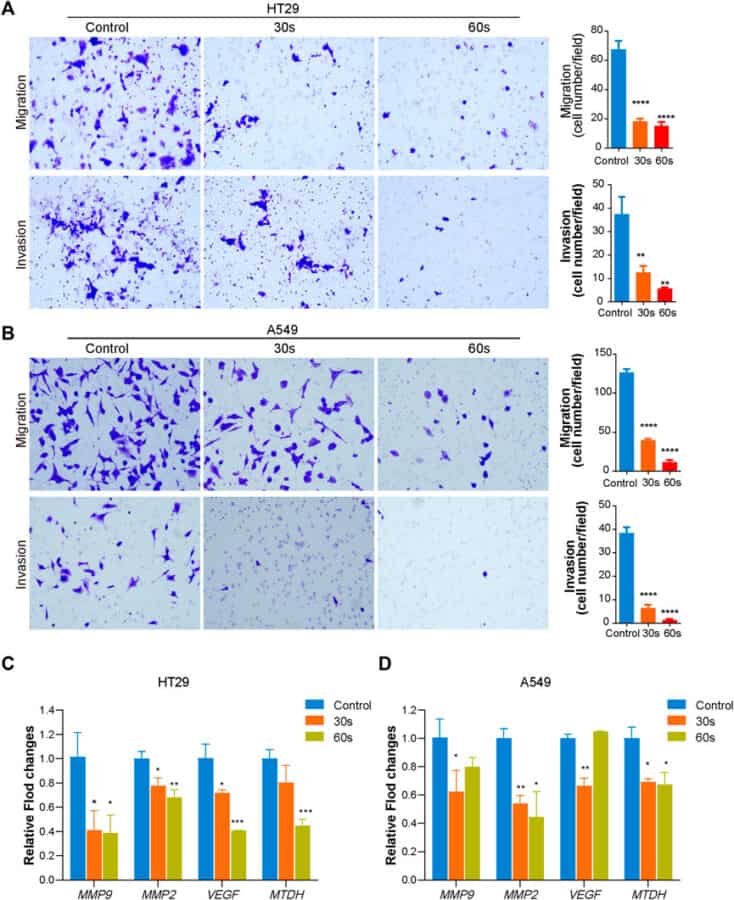
Die HT29 (A) und A549 (B) Zellen wurden mit dem PZ2 für 30 und 60 Sekunden bearbeitet, für 24 h inkubiert, bevor sie anschließend dem Transwell-Migrations- und Matrigel-Invasion-Test unterzogen wurden. In Abbildung 2 sind repräsentative Bilder (links) und Statistiken (rechts) des Migrations- und Invasionsassays zu sehen. Der Maßstabsbalken entspricht 200 μm. Die Experimente wurden dreifach durchgeführt.
Die Plasma-induzierte Apoptose in den HT29- und A549-Zellen wurde unter Verwendung der AO/EB-Färbung gekoppelt mit der Durchflusszytometrie bestätigt und die Produktion von Apoptose-verwandten Proteinen wie Cytochrom c, PARP, gespaltener Caspase-3 und Caspase-9, Bcl-2 und Bax, wurde unter Verwendung von Western-Blotting verifiziert.
Die Ergebnisse der Plasma-Behandlung in in-vitro-Tests wurden in vivo unter Verwendung von Xenotransplantat-Mäusen getestet. Die Antikrebswirkung wurde bestätigt und der CAP-vermittelten Apoptose zugeschrieben. Die immunhistochemische Analyse ergab, dass die Expression von gespaltener Caspase-9, Caspase-3, PARP und Bax hochreguliert war, während die von Bcl-2 nach der CAP-Behandlung herunterreguliert wurde. Diese Ergebnisse deuten zusammenfassend darauf hin, dass die Aktivierung des mitochondrialen Signalwegs während der CAP-induzierten Apoptose menschlicher Dickdarm- und Lungenkrebszellen in vitro und in vivo beteiligt ist.
Den gesamten Beitrag „Induzierte Apoptose durch kalt atmosphärisches Plasma in menschlichen Dickdarm- und Lungenkrebszellen“ finden Sie hier.




